공기극에서 산소의 환원반응에 의해 생성된 산소이온이 전해질을 통해 연료극으로 이동하여, 다시 연료극에 공급된 수소와 반응함으로써 물을생성하게 되며, 이때 연료극에서 전자가
생성되고 공기극에서 전자가 소모되므로 두 전극을 서로 연결하여 전류를 발생시키는 발전기술
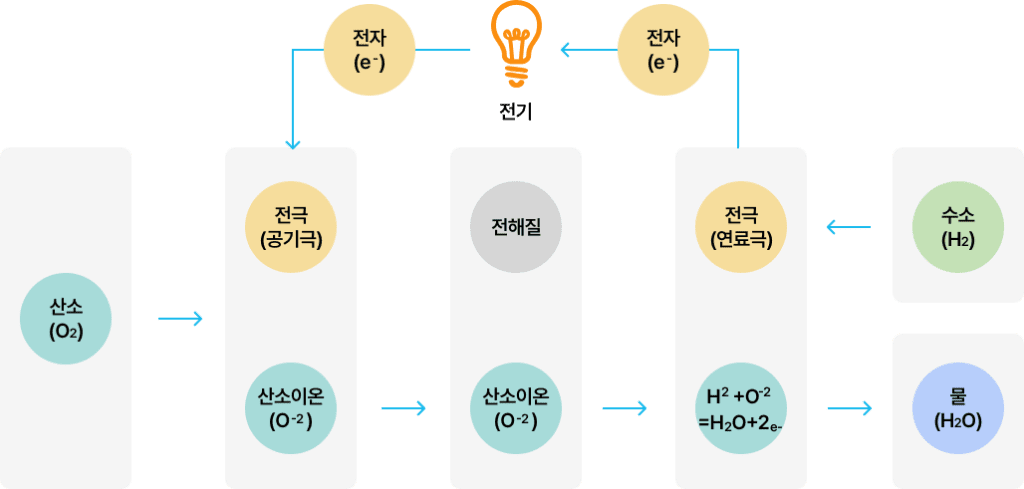
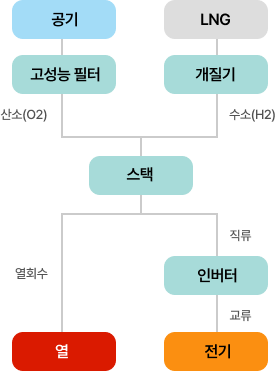
공기극에서 산소의 환원반응에 의해 생성된 산소이온이 전해질을 통해 연료극으로 이동하여, 다시 연료극에 공급된 수소와 반응함으로써 물을생성하게 되며, 이때 연료극에서 전자가 생성되고 공기극에서 전자가 소모되므로 두 전극을 서로 연결하여 전류를 발생시키는 발전기술

| 구분 | 고온형 연료전지 | 저온형 연료전지 | ||||
| 용융탄산염 (MCFC) | 고체산화물 (SOFC) | 인산염 (PAFC) | 알칼리 (AFC) | 고분자전해질형 (PEMFC) | 직접메탄올 (DMFC) | |
| 작동온도 | 550~700°C | 600~1,000°C | 150~250°C | 50~120°C | 50~100°C | 50~100°C |
| 촉매 | 회티타늄 | 니켈 | 백금 | 니켈 | 백금 | 백금 |
| 전해질 | 탄산염 | 세라믹 | 인산염 | 수산화칼슘 | 이온교환막 | 이온교환막 |
| 전력생산효율 | 45~50 | 50~60 | 40~45 | – | <40 | – |
| 설치용도 | 대규모발전, 중•대형 건물 | 대규모발전, 소•중•대용량 | 중형건물 | 우주발사체 | 수송용, 가정용, 휴대용 전원 | 휴대용 전원 |
| 특징 | 발전효율 높음, 내부개질 가능, 열병합대응 가능 | 발전효율 높음, 내부개질 가능, 복합발전 가능 | CO내구성 큼, 열병합대응 가능 | – | 저온작동, 고출력밀도 | 저온작동, 고출력밀도 |
| 구분 | 용융탄산염 (MCFC) | 고체산화물 (SOFC) |
| 작동온도 | 550~700°C | 600~1,000°C |
| 촉매 | 회티타늄 | 니켈 |
| 전해질 | 탄산염 | 세라믹 |
| 전력생산효율 | 45~50 | 50~60 |
| 설치용도 | 대규모발전, 중•대형 건물 | 대규모발전, 소•중•대용량 |
| 특징 | 발전효율 높음, 내부개질 가능, 열병합대응 가능 | 발전효율 높음, 내부개질 가능, 복합발전 가능 |
| 구분 | 인산염 (PAFC) | 알칼리 (AFC) |
| 작동온도 | 150~250°C | 50~120°C |
| 촉매 | 백금 | 니켈 |
| 전해질 | 인산염 | 수산화칼슘 |
| 전력생산효율 | 40~45 | – |
| 설치용도 | 중형건물 | 우주발사체 |
| 특징 | CO내구성 큼, 열병합대응 가능 | – |
| 구분 | 고분자전해질형 (PEMFC) | 직접메탄올 (DMFC) |
| 작동온도 | 50~100°C | 50~100°C |
| 촉매 | 백금 | 백금 |
| 전해질 | 이온교환막 | 이온교환막 |
| 전력생산효율 | <40 | – |
| 설치용도 | 수송용, 가정용, 휴대용 전원 | 휴대용 전원 |
| 특징 | 저온작동, 고출력밀도 | 저온작동, 고출력밀도 |

